
-
2024-8-13
嚙齒動(dòng)物血生化項目分析(下)
-
2024-8-6
小二麻痹癥與百萬(wàn)只猴
-
2024-7-30
非人靈長(cháng)類(lèi)動(dòng)物源的傳染病
-
2024-7-23
實(shí)驗動(dòng)物術(shù)后監測及切口閉合的原則
-
2024-7-16
獸醫流行病學(xué)在規模化猴場(chǎng)疾病防控中的應用
-
2024-7-9
嚙齒動(dòng)物血生化項目分析(上)
-
2024-7-2
實(shí)驗嚙齒動(dòng)物手術(shù)操作的止痛方案考量
-
2024-6-25
混亂的圈養食蟹猴遺傳組成
-
2024-6-18
規模化猴場(chǎng)傳染性疾病防控設想
-
2024-6-11
小鼠肺部插管簡(jiǎn)易方法
如果實(shí)驗設計不嚴謹——以漸凍人癥轉基因小鼠藥物研發(fā)為例
肌萎縮性脊髓側索硬化癥

因中樞神經(jīng)系統內控制骨骼肌運動(dòng)的神經(jīng)元退化導致的肌萎縮性脊髓側索硬化癥(Amyotrophic lateral sclerosis: ALS,也稱(chēng)漸凍人癥)是一種漸進(jìn)且致命的神經(jīng)退行性疾病。由于運動(dòng)神經(jīng)元退化和死亡,肌肉逐漸萎縮致大腦完全喪失控制隨意運動(dòng)的能力,最終會(huì )造成發(fā)音、吞咽,以及呼吸和運動(dòng)障礙。著(zhù)名物理學(xué)家霍金就是一名ALS患者。目前還沒(méi)有真正可有效治療ALS的藥物和方法。
絕大多數(90-95%)的ALS發(fā)病原因不明,但也有約5-10%的ALS患者表現出了家族遺傳性,其中超氧化物歧化酶 1(Superoxide Dismutase 1:SOD1)基因突變約占這些遺傳性ALS病例的10%。SOD1也是第一個(gè)被鑒定出來(lái)的ALS風(fēng)險基因[1],因此很快就有科學(xué)家構建了一種含有第93位甘氨酸突變?yōu)楸彼幔℅93A)的人SOD1基因的轉基因小鼠模型,全名為B6SJL-Tg(SOD1*G93A)1Gur/J轉基因小鼠[2]。該轉基因小鼠基因組中被轉入了23個(gè)拷貝的人源SOD1*G93A突變基因,接下來(lái)我們將其簡(jiǎn)稱(chēng)SOD1*G93A轉基因小鼠。

圖二:SOD1*G93A轉基因小鼠是以B6和SJL雜交子代為背景品系,通過(guò)原核注射和胚胎移植得到的轉基因小鼠模型,因此其毛色多樣,圖片來(lái)自Jax實(shí)驗室(https://www.jax.org/strain/002726)
自1996年SOD1*G93A轉基因小鼠問(wèn)世以后,其就被廣泛應用于A(yíng)LS藥物研發(fā)的臨床前動(dòng)物試驗中。到2004年,短短8年時(shí)間內,已至少有50篇文章描述了從小分子到病毒載體的各類(lèi)ALS治療方案,可延長(cháng)SOD1*G93A轉基因小鼠的壽命,其中最長(cháng)可以延長(cháng)壽命100天(78%的壽命延長(cháng))。這些藥物很快進(jìn)入臨床試驗,然而,迄今為止,除了利魯唑(最多延長(cháng)ALS患者兩個(gè)月壽命)之外,沒(méi)有任何一種藥物顯示出對人類(lèi)ALS疾病的進(jìn)程有顯著(zhù)影響[3]。這給醫藥公司帶來(lái)了巨大損失,如2008年在美國國家科學(xué)院院刊上發(fā)表的一篇文章顯示鋰可以將SOD1*G93A轉基因小鼠的存活時(shí)間延長(cháng)30天[4]。由于鋰早已經(jīng)被用于治療精神分裂癥,許多ALS患者開(kāi)始超說(shuō)明書(shū)服用該藥物,希望減緩疾病進(jìn)程。然而,招募了數百名患者,花費了遠超1億美元的三個(gè)同時(shí)啟動(dòng)的獨立III期臨床試驗結果卻顯示鋰對ALS無(wú)任何治療效果。
其實(shí)不僅僅是ALS的藥物研發(fā),在整個(gè)醫藥研發(fā)領(lǐng)域,動(dòng)物實(shí)驗結果的平均臨床轉化率也是非常低的,平均在11%左右 。那么到底是什么原因導致了如此高比例的動(dòng)物實(shí)驗結果無(wú)法實(shí)現在人類(lèi)的臨床轉化呢?
1999年,美國麻省理工學(xué)院的機械工程師詹姆斯·海伍德在得知他的哥哥史蒂芬·海伍德被確診患有ALS,并無(wú)任何有效治療方法后,與家人一起創(chuàng )立了一家非盈利性生物技術(shù)公司,即ALS 治療開(kāi)發(fā)研究所 (ALS-TDI)。ALS-TDI成立后開(kāi)展了一項旨在尋找SOD1*G93A轉基因小鼠實(shí)驗結果臨床轉化失敗原因的項目,即使用SOD1*G93A轉基因小鼠重復已發(fā)表科研論文中的動(dòng)物實(shí)驗,以找出其臨床轉化失敗的原因。
在A(yíng)LS-TDI開(kāi)展的重復性實(shí)驗中,他們不僅嚴格執行盲法對照,而且對給藥組和對照組的動(dòng)物進(jìn)行了更為精細的分配和動(dòng)物篩查以排除系統誤差。他們分組及實(shí)驗要求包括:
⑴ 年齡匹配;
⑵ 性別匹配;
⑶ 同窩匹配:即使用同一天出生的同一非轉基因母親和轉基因父親的后代進(jìn)行分組,具體來(lái)說(shuō),治療組中的每個(gè)雄性(和雌性)在對照組中都有一個(gè)同窩兄弟(和姐妹);
⑷ 樣本量設定:每組使用動(dòng)物數量為24只(12雌,12雄);
⑸ 死因篩查:檢查記錄每一只動(dòng)物的死亡原因,排出非ALS致死個(gè)體;
⑹ 轉基因拷貝數監控:有研究證明SOD1*G93A轉基因小鼠在傳代過(guò)程中會(huì )出現轉基因拷貝數丟失的現象,且低拷貝的轉基因小鼠的平均壽命會(huì )加長(cháng)。
在這一嚴格實(shí)驗分組和動(dòng)物篩查條件下,ALS-TDI的科研人員總共使用了5429只SOD1*G93A轉基因小鼠測試了包括利魯唑在內的100多種(大部分已有論文發(fā)表并證明可延長(cháng)SOD1*G93A轉基因小鼠壽命)候選化合物,卻沒(méi)有發(fā)現任一化合物表現出可延長(cháng)SOD1*G93A轉基因小鼠壽命的效果(圖三)。
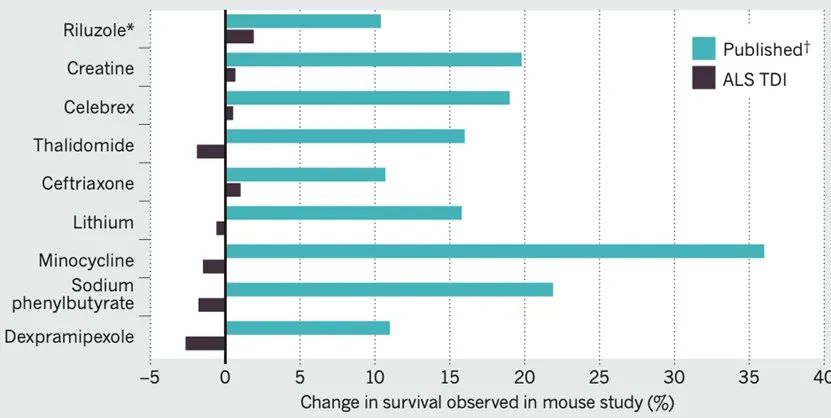
圖三:ALS-TDI以SOD1*G93A轉基因小鼠開(kāi)展的重復實(shí)驗結果與已發(fā)表實(shí)驗結果對比[3]
為找出導致那些已經(jīng)發(fā)表實(shí)驗結果無(wú)法被重復的原因,他們以在A(yíng)LS-TDI開(kāi)展實(shí)驗中所使用的2000多只對照小鼠作為研究對象,進(jìn)行了計算機分組模擬實(shí)驗。由于這些小鼠從出生到死亡及死亡原因的信息在A(yíng)LS-TDI都有詳細的記錄,因此他們能夠以所有對照小鼠為數據庫,分析前述重復實(shí)驗中設定的不同分組和動(dòng)物篩查條件對實(shí)驗結果的影響。即通過(guò)計算機對這些沒(méi)有經(jīng)過(guò)任何藥物處理的小鼠進(jìn)行分組,將一組設為假定的實(shí)驗組,而另一組設為假定的對照組,然后依據已有的小鼠死亡時(shí)間記錄,統計兩組小鼠之間是否存在顯著(zhù)差異。經(jīng)過(guò)多次重復,計算出現5%以上顯著(zhù)差異的百分比。由于這些對照小鼠沒(méi)有接受過(guò)任何化合物處理,因此如果假定的實(shí)驗組和對照組中出現了顯著(zhù)性差異,那么其來(lái)源應該是分組時(shí)的系統誤差。
結果顯示,在樣本量大小為4的計算機分組模擬對比實(shí)驗中,在隨機分組和不進(jìn)行死因篩查及排除低轉基因拷貝數個(gè)體條件下,兩組間出現顯著(zhù)差異的可能性超過(guò)了50%。而隨機分組的同時(shí)進(jìn)行死因篩查并排除低轉基因拷貝數個(gè)體和進(jìn)行性別匹配的分組條件下,樣本量為4的模擬分組實(shí)驗中也有30%的可能出現兩組死亡時(shí)間的顯著(zhù)差異(圖四)。隨著(zhù)樣本量的增加,出現顯著(zhù)性差異的可能性逐漸減少,但要實(shí)現低于5%(統計學(xué)上通常設置的顯著(zhù)置信區間)的顯著(zhù)性差異,樣本量要達到每組24只動(dòng)物。如果不做分組條件控制,即使樣本量到50只也難以排除系統誤差。
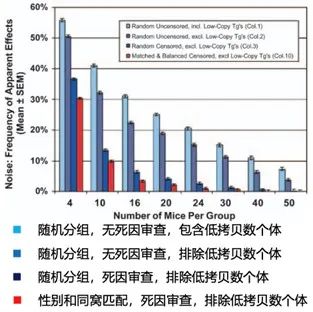
圖四:分組條件導致的系統誤差[3]
ALS- TDI的這個(gè)計算機模擬實(shí)驗結果說(shuō)明,前述那些已經(jīng)發(fā)表的基于SOD1*G93A轉基因小鼠實(shí)驗結果無(wú)法實(shí)現臨床轉化的真正原因極大可能源于其實(shí)驗設計的不合理。這些實(shí)驗因為沒(méi)有排除分組時(shí)的系統誤差而導致了假陽(yáng)性結果。這個(gè)研究也暴露了當下使用實(shí)驗動(dòng)物開(kāi)展研究的諸多問(wèn)題,如盲目地追求減少使用動(dòng)物的數量;對所用動(dòng)物遺傳、微生物和繁殖等特性不了解;實(shí)驗過(guò)程中對動(dòng)物關(guān)注不夠,不清楚動(dòng)物發(fā)病或死亡的真正原因等。這些問(wèn)題不僅僅需要引起實(shí)驗動(dòng)物從業(yè)人員的注意,科研人員同樣需要給予關(guān)注。因為實(shí)驗設計不嚴謹導致的假陽(yáng)性結果不僅是人力、物力和財力的巨大浪費,也嚴重有違動(dòng)物實(shí)驗倫理福利,這樣的實(shí)驗不會(huì )帶來(lái)科學(xué)進(jìn)步,且浪費了大量實(shí)驗動(dòng)物的生命。比如在A(yíng)LS-TDI開(kāi)展的無(wú)法重復出已發(fā)表結果的實(shí)驗中,那些已經(jīng)發(fā)表的工作累計使用小鼠的數量就超過(guò)了18000只。此外,在動(dòng)物實(shí)驗倫理申請時(shí)常用替代、優(yōu)化和減少(俗稱(chēng)3R原則)原則來(lái)指導倫理審查工作,有時(shí)為了滿(mǎn)足3R原則中的“減少”原則,加上開(kāi)展實(shí)驗成本的考慮,往往選擇使用最少的動(dòng)物數量(比如多為每組6只),但從ALS-TDI的這個(gè)研究看,樣本量過(guò)小,會(huì )導致系統誤差加大,因此極大可能出現假陽(yáng)性結果。這個(gè)時(shí)候大家或許忘了3R原則使用的大前提是要能夠實(shí)現擬開(kāi)展實(shí)驗的科學(xué)目標,如果單純?yōu)榱恕皽p少”而使用更少的實(shí)驗動(dòng)物導致科學(xué)目標無(wú)法實(shí)現,那不是減少,而是對動(dòng)物生命的漠視。
參考文獻:
1.Rosen DR, Siddique T, Patterson D, Figlewicz DA, Sapp P, Hentati A, Donaldson D, Goto J, O'Regan JP, Deng HX, et al.: Mutations in Cu/Zn superoxide dismutase gene are associated with familial amyotrophic lateral sclerosis. Nature 1993, 362:59-62.
2.Tu PH, Raju P, Robinson KA, Gurney ME, Trojanowski JQ, Lee VM: Transgenic mice carrying a human mutant superoxide dismutase transgene develop neuronal cytoskeletal pathology resembling human amyotrophic lateral sclerosis lesions. Proc Natl Acad Sci U S A 1996, 93:3155-3160.
3.Scott S, Kranz JE, Cole J, Lincecum JM, Thompson K, Kelly N, Bostrom A, Theodoss J, Al-Nakhala BM, Vieira FG, et al: Design, power, and interpretation of studies in the standard murine model of ALS. Amyotroph Lateral Scler 2008, 9:4-15.
4.Fornai F, Longone P, Cafaro L, Kastsiuchenka O, Ferrucci M, Manca ML, Lazzeri G, Spalloni A, Bellio N, Lenzi P, et al: Lithium delays progression of amyotrophic lateral sclerosis. Proc Natl Acad Sci U S A 2008, 105:2052-2057.
5.Kola I, Landis J: Can the pharmaceutical industry reduce attrition rates? Nat Rev Drug Discov 2004, 3:711-715.
6.Hay M, Thomas DW, Craighead JL, Economides C, Rosenthal J: Clinical development success rates for investigational drugs. Nat Biotechnol 2014, 32:40-51.


